就活や転職をするにも業界のことをある程度知っていないと何が自分にとって合っている仕事なのかを考えることも難しいでしょう。
そこで今回の記事では、治験の業界のことについて全く知らい方にも業界のことが分かるよう分かりやすくまとめた記事を書いてみました。
また、CRA(臨床開発モニター)という仕事に興味を持っている方向けにCRAの業界での立ち位置についても触れているので、ご覧ください。
治験とは何か?
治験とは、臨床試験の一種で、その中でも医薬品や医療機器を厚生労働省などの当局に承認してもらう目的で実施する臨床試験のことを指します。
これだけ説明をしただけでは、今一よく分からないと思いますので、もう少し噛み砕いて説明をしていきます。
今、日本で発売されている薬はすべて、有効性や安全性についてしっかりと確認され、厚生労働省で承認されたものになります。
効果が無いのに販売していたり、効果はあるけど、とても危険な薬が世に出回ってしまったら当然みなさんにとって不利益なことですよね?
世に出る医薬品は、有効性と安全性がしっかりと保証されている必要がありますが、その有効性や安全性は以下のような順番で調べていきます。
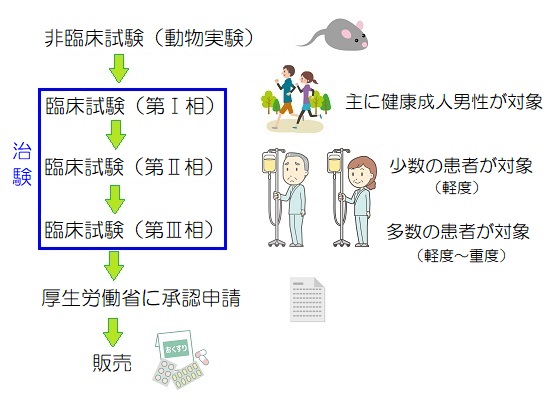
上の図のように、まずは動物実験で有効性や安全性を調べ、安全であるという結果が出たらヒトで有効性や安全性を確かめていきます。
ヒトで有効性や安全性を確かめるときは、少し複雑なのですが、単純にヒトで有効性や安全性を確かめることを臨床試験と言い、その中でも、医薬品として承認をもらうために実施する臨床試験のことを治験と言います。
また、臨床試験と似たようなことばで臨床研究というものもあります。
使い分けるには少々慣れが必要なので、ここはぼんやり理解していれば良いかと思いますが、それぞれの意味も少し説明しておきます。
臨床研究と臨床試験と治験の違い
「臨床研究」というのは、ヒトを対象にした研究全部をひっくるめての言い方になります。
そのうちの侵襲性(対象者に負荷を与えるもの)や介入(通常の処置以外に何かしらの措置を加えること)を伴うものを「臨床試験」、そしてその中でも更に医薬品・医療機器の承認申請のために実施するものを「治験」と言います。
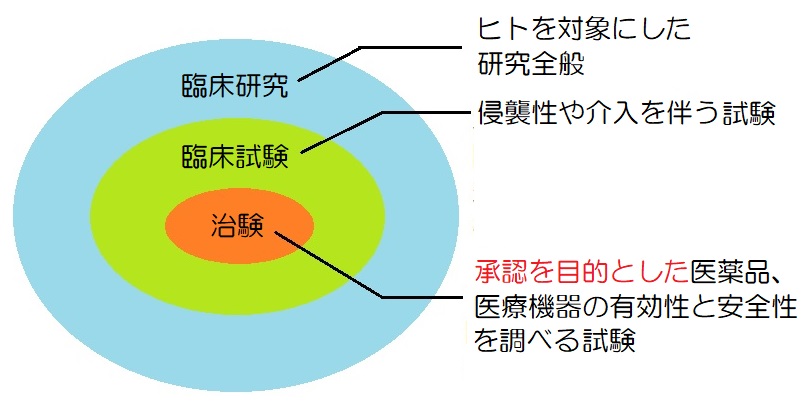
もっとイメージがしやすいようにそれぞれについて具体例を見ていきましょう。
臨床研究の具体例
この調査は、過去のカルテの情報から患者さんのデータを参照しているだけなので、介入や患者さんへの侵襲性が無いので、臨床試験でも治験でもなく臨床研究となります。
臨床試験の具体例
新しく開発した血糖値を下げる効果が期待される健康食品の効果を調べるために、健康食品を食べた人と健康食品を食べなかった人での血圧の変化の差を調査。
この調査では、血糖値を測定するために採血をすることになりますが、その採血が「侵襲性」に該当します。侵襲性がある試験ではあるもの、医薬品ではなく健康食品の効果を確かめる調査なので、治験には該当せず臨床試験ということになります。
治験の具体例
血糖値を下げる効果が期待される新薬の効果と安全性を調べるため、実役群とプラセボ(偽薬)群でどのような差があるのかを調査。
この調査では、承認を取得する為に新薬の有効性と安全性を調査しているので、臨床試験には該当性せず治験ということになります。
世間一般では、よく「化粧品の治験」とか「健康食品の治験」と言ったような使い方がされていますが、どちらも医薬品でも医療機器でも無いので治験というのは間違っているということですね。
正しくは、「化粧品の臨床試験」、「健康食品の臨床試験」となるわけです。
CRAの他に、健康食品の会社や化粧品の会社にも就職を考えている場合は覚えておいた方が良いです。
面接で話に出てきた機会があったとき、しっかりとした認識で言葉を使っていれば印象は全然違います。
治験の中でも色々と種類がある
今回は治験についての記事なので、治験についてもう少し深く掘り下げていきます。
医薬品を開発するときには非臨床試験で安全性を調査して、そのあと臨床試験である治験で有効性と安全性を調べていきますが、治験は大きく分けてI相~III相の3段階に分かれています。
そのそれぞれで、対象となる方や目的が異なってきます。
| 開発相 | 調査内容 | 対象 |
|---|---|---|
| 第I相 | 安全性・薬物動態 | 健康成人男性 |
| 第II相 | 用法用量・有効性・安全性 | 少数の軽度の患者 |
| 第III相 | 有効性・安全性 | 多数の軽度~重度の患者 |
第I相試験は、健康成人男性を対象にすることがほとんどで、世間一般で言われているような「治験のバイトで稼ぐぜ!」というようなときに使われている「治験」がこの第I相の治験になります。
ちなみにですが、「治験のバイト」という言い方は、医薬品業界では絶対に使ってはいけませんのでご注意を。
CRAの面接でもし「治験のバイト」という言葉を使ってしまったら場合によってはそれだけで落ちることもあるかもしれません。
詳しいことはまた別記事でまとめているので、気になる方は読んでみて下さい。
第I相では健康成人男性を対象に主に安全性について調べます。
非臨床試験(動物実験)の後の最初にヒトに薬を投与するので、ファースト・イン・ヒューマン試験とも呼ばれており、特に治験薬の投与量についてはとても慎重に考慮して行われるべき治験になります。
第I相試験で安全性に問題が無いことが分かったら、いよいよ患者さんに対しての投与が始まります。
患者さん(男女どちらも)は、当然、健康成人男性よりは体が弱い訳ですので、いきなり重症の患者さんに治験薬を投与する訳にはいきません。
そこで、第II相試験では、症状が軽度の比較的少数の患者さんを対象に安全性と有効性を見ることが一般的です。
具体的には、安全性と有効性がしっかりと担保できる治験薬の用法・用量を調べる目的のものも多く、用量設定試験と呼ばれることもあります。
そして、治験の最終段階である第III相では、軽度~重度など様々な症状の範囲で比較的多数の患者さんを対象に安全性と有効性を調べていきます。
第III相試験が終わったら、統計解析をして有効性と安全性についてまとめ、厚生労働省の承認審査が始まり、めでたく承認されたら世の中に流通していくことになります。
1つの医薬品を0から開発するには、9~17年かかると言われていて、その最終段階が治験であり、その治験に深く関わるのがCRAということになります。
治験に登場する役割別の解説

次に治験をするうえで登場する役割について紹介をしていきたいと思います。
治験での役割は、大きなくくりで考えると製薬会社側と医療機関側の2つの立場に分けられます。
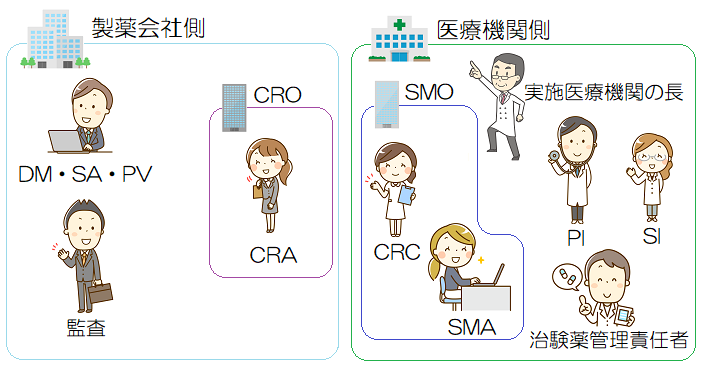
もちろん今回紹介する以外にも治験に関わっている方はいるのですが、全てを載せると物凄いボリュームになってしまうので、今回は主な役割について紹介をしていきます。
CRA
CRA(臨床開発モニター:Clinical Research Associate)とは、治験の実施医療機関において治験が適切に実施されているかを製薬企業側の立場から確認する役割の職業になります。治験が適切に実施されているかを確認する他にも、医療スタッフ向けに治験についての説明会の実施や治験薬・治験資材の搬入手続きなど治験に関連した幅広い業務を担っています。
CRAの担当施設で疑義事項があった場合などは、医師に面会をして確認をしたりすることもあり、スーツで病院にいることが多いため、よく営業(MR)と間違われることがあります。
CRAは製薬会社側の立ち位置になりますが、CRO(開発業務受託機関:Contract Research Organization)という会社が製薬会社から委託を受けて業務をしていることが最近では多くなってきました。
DM
DM(データマネージメント:Data Management)とは、治験の実施医療機関で入力された治験のデータを集積するシステムであるEDC(Electronic Data Capture)の管理・運用をする職業になります。
治験の開始時点では、治験実施計画書や試験として収集すべき情報を網羅したり、治験実施計画書からの逸脱を検知できるようなロジックを組んだりするお仕事がメインであり、DMの仕事の精度が治験のデータ収集の制度に大きく影響すると言えるでしょう。
また、被験者が本格的に組み入れられてからは、各実施医療機関がEDCに入力するデータが適切であるかを管理し、EDCの入力方法など施設やCRAからの問い合わせの対応を行います。
そして、試験終盤ではEDCに入力されたデータの質を確認し、データベースロックという形で治験のデータを固定する役割を担っています。
治験のデータを扱うお仕事ですので、DMの仕事は精度が非常に重要視される傾向にあります。
また、DM業務は内勤業務がメインになります。
SA(STAT)
SA(統計解析:Statistical Analysis)とは、治験によって収集されたデータを統計解析して、医薬品の有効性や安全性を検証する職業になります。
治験のデータ解析に関わるだけではなく、市販後のデータ解析にも関わるため扱っている範囲は広めです。
統計解析のチームは、製薬メーカーの場合、試験のデザインを考える段階から関与し、治験で収集するサンプル数や有効性や安全性を評価する上で最も適切な統計手法をPMDAと議論する際にも登場します。
また、治験の最終段階では治験で収集されたデータを解析し、その解析結果について他部署と一緒に考察をおこなうため、医薬品開発の幅広い部分に携われる職種でもあります。
私個人の感覚ですが、統計解析の方はどの統計解析手法を使うのが妥当かを導き出すのにセンスがとても影響する職種だとも思っています。
既成概念に捉われず、チャレンジングな発想を持っている方が活躍できるのではないかと感じています。
なお、STATもDMと同様に内勤業務がメインです。
PV
PV(安全性情報:Pharmacovigilance)とは、開発中~発売後の医薬品の副作用などの安全性情報を取り扱う職業になります。治験では、治験薬によって生じた重篤な副作用情報を当局に報告するなどの業務があります。
治験薬の安全性に関わる部署であるため、治験で発生している副作用についてはしっかりと把握しており、疾患に対する知識も豊富にあります。
そのため、会社によっては医師がチームに入っていることもあり、臨床的な知識レベルは非常に高いと言えます。
なお、治験だけではなく市販後の安全性情報も扱っているため、その業務範囲は広範に渡ります。
MW
MW(メディカルライティング:Medical Writing)は、治験で発生する様々な資料を作成する職業になります。
具体的には以下のような治験の資料を作成します。
●治験実施計画書(プロトコール)
●総括報告書(治験のデータをまとめた資料)
●申請資料(PMDAに提出する資料)
Medical Writingは、それぞれの資料をただ単純にPCで作るだけの事務的なお仕事ではなく、しっかりと内容まで精査をするような職業ですので専門的な知識が求められます。
具体的には、統計学の知識や薬事規制に関する知識などが求められ、更には非臨床のデータもまとめなければいけないためその知識の幅は非常に広いのが特徴です。
働き方としては、CRAとは対照的にほぼ全てが内勤業務となります。
監査
監査(Audit)とは、製薬会社側の立場で、治験の実施医療官で適切に治験が実施され、かつその質が担保されているかを確認する職業になります。CRAと似ていますが、監査はCRAがしっかりと治験の実施医療機関のことをしっかりと確認をして質が担保できているかについても確認をしている点でCRAとは異なります。
そのため、CRAが所属する臨床開発部とは別の独立した部署に所属しており、第三者的な立場から治験の実施状況を確認するという立場になります。
監査についても大手CROで業務委託をしていることがありますが、CRA程メジャーではありません。
CRC
CRC(治験コーディネーター:Clinical Research Coordinator)とは、治験の実施医療機関において治験が適切にそして円滑に実施することができるよう治験責任医師の業務の補助をする職業になります。
具体的には、治験に参加しようとする候補者に治験の補助説明をしたり、医療機関に訪問をしてくるCRAの対応にあたったりします。
治験は、CRCの存在無しでは適切に進めていくことは非常に困難で、治験を成功させるにはとても重要な存在になります。
CRCは、大学病院などの大規模な医療機関の場合、院内CRCという医療機関に雇用されているCRCがいますが、最近ではSMO(治験施設支援機関:Site Management Organization)に所属していて医療機関から委託を受けて業務を実施しているパターンもあります。
CRCについては、2018年にTBSで放映されたドラマ『ブラックペアン』にも登場して世間の認知度も以前よりは上がってきています。
ただし、ブラックペアンで描かれているCRCは色々と物議を醸しており、日本薬理学会がTBSに抗議文を送るような事態にまで発展しました。
もしみなさんがブラックペアンに登場するCRCを想像されているのであれば、実際には全然違うのでお気を付けください!
SMA
SMA(治験事務局担当者:Site Management Associate)とは、治験の実施医療機関において治験に関連して発生した書類を整備・管理するのが主な業務になります。CRAが、治験関連書類が適切に保管されているかを確認しに来る際に対応するという業務もあります。
SMAは、医療機関で発生する書類の管理をするため、製薬気企業側のCRAよりも医療機関側のCRCと関わることが多くあります。
また、SMAもCRCと同じくSMOが医療機関から業務を受託して業務をしていることもあります。
実施医療機関の長
実施医療機関の長とは、治験を実施するうえで主に手続き関連の対応をする役割を担っており、院長のことを指すことが一般的です。治験関連資料(例えば、治験に関する契約書類など)に名前が載ることがありますが、実際に現場に出て何か作業をするということはあまりありません。
CRAとしても、実施医療機関の長と面会をするということもほぼありません。
治験責任医師
治験責任医師(PI:Principal Investigator)とは、治験ごとに定められており、その治験に対する医療機関側の責任者になります。
治験での医学的な判断について責任を負う役割があるほか、治験に参加する候補者向けの同意説明文書を作成したり、治験で生じた重篤な副作用について評価をするという重要な役割があります。
CRAが被験者について何か問い合わせがある際には治験責任医師と面会することもよくあり、CRAが最もよく面会する医師と言えるでしょう。
治験分担医師
治験分担医師(SI:Sub Investigator)とは、治験責任医師によって治験の業務の分担をされた医師のことを指します。
治験行為(治験に関連すうる診察など)は、治験責任医師か治験分担医師しかすることができません。そのため、被験者の主治医を治験分担医師とすることもよくあります。
治験責任医師と比べるとCRAが面会をする頻度は少ない傾向にありますが、治験参加者の主治医である場合は、問い合わせをする際に治験分担医師と面会をすることもあります。
治験薬管理責任者
治験薬管理責任者とは、治験実施医療機関に搬入される治験薬の管理・責任を担っている役割の方を指します。
医療機関に薬剤科がある場合には、薬剤部長がこの役割を担っていることが一般的です。
CRAとしては、治験薬管理責任者から業務を分担される治験薬管理者と打ち合わせをして、治験薬の搬入日の調整をしたりします。
治験関連で重大な事故も起きている

治験では、イギリスでのTGN1412事件やフランスでのレンヌ事件など、治験に関する様々な事故が起きています。
2019年には、エーザイのE2082の第I相(健康成人大生対象)の治験において、治験に参加した被験者が死亡するという痛ましいニュースがありました。
どんな優秀な薬にも必ず副作用はあります。
特にヒトでの投与データがほとんどない段階でおこなわれる治験については、しっかりと厳格に管理されるべきです。
日本では、薬機法やGCP省令など治験に関するルールも定められていますが、それだけではやはり防ぎきれない部分があるので、先ほど紹介した治験に関連した役割の方全員でしっかりと管理をして事故を無くしていくことが重要と言えるでしょう。
2019年にエーザイのE2082の治験で成人男性が治験薬投与後に死亡したというショッキングなニュースが流れました。 各SNSでも「治験バイトで死亡とかヤバくない!?」というコメントが溢れ、治験に対して怖いと思われた方もい …
まとめ
治験について詳しく説明をしてみましたがいかがだったでしょうか。
治験については、この記事には書ききれないことがまだ山ほどあります。
この記事を読まれている方には色々な方がいるかと思いますが、これから製薬企業やCROに就職しようと考えている方は治験のおおまかな流れについては、面接前などに把握しておくことをおすすめします。



の面接対策についてまとめてみた.jpg)